卡培他滨是一种新型的口服化疗药物,诸多的临床研究证实卡培他滨与持续静脉滴注的氟尿嘧啶疗效相等。虽然手足综合征发生的比例升高,但是大部分患者耐受,而且对骨髓抑制较轻,用药方便也是卡培他滨相对于静脉用药的优势之一。
已有研究探讨了口服卡培他滨在结直肠癌中替代静脉用氟尿嘧啶(5-FU)。研究证实,卡培他滨联合奥沙利铂(XELOX)方案在转移性结直肠癌一线治疗中表现出与亚叶酸钙、5-FU和奥沙利铂(FOLFOX)方案相当的疗效与安全性,并且XELOX方案使用更方便,且在血液方面的安全性也更具优越性。
对于转移性结直肠癌(mCRC)的二线治疗,基于亚叶酸钙、5-FU和伊立替康联合化疗方案(简称FOLFIRI)是目前国际指南推荐的标准化疗方案之一。研究表明,与FOLFIRI方案相比,卡培他滨联合伊立替康(XELIRI)方案可显著延长无进展生存(PFS)期。然而XELIRI方案由于毒副反应较大,尤其是III/度腹泻发生率明显升高,因而在一定程度上限制了XELIRI方案的临床应用。
随后,研究人员修改了XELIRI方案以达到更可行的剂量——降低伊立替康(第1天,200 mg/m2)和卡培他滨(第1~14天,1600 mg/m2)剂量的改良XELIRI(mXELIRI)方案。在一线和二线治疗中,与XELOX联合贝伐珠单抗(Avastin)方案相比,mXELIRI联合贝伐珠单抗联合显示出良好的耐受性和疗效。
来自中山大学附属肿瘤医院的徐瑞华教授领衔中日韩研究者团队开展了AXEPT研究。这是一项评估mXELIRI vs FOLFIRI联合或不联合贝伐珠单抗治疗转移性结直肠癌患者的疗效和安全性的多中心、开放标签、随机III期临床试验,旨在证实作为二线治疗转移性结直肠癌的方案,含卡培他滨的治疗方案在总生存方面的非劣效性。
研究方法
该研究共招募了来自日本,中国和韩国的98家医院650例患者,这些患者年龄在20岁或以上,组织学证实为不可切除的结直肠腺癌,并且已经退出一线化疗治疗的转移性结直肠癌。
患者以1:1的比例随机分配至接受mXELIRI联合或不联合贝伐单抗(第1天静脉注射伊立替康200 mg / m2加上第1-14天每天两次口服卡培他滨800 mg / m2,每21天重复一次,有或无(第1天静脉注射贝伐单抗7.5 mg / kg)或FOLFIRI联合或不联合贝伐单抗(第1天静脉注射伊立替康180 mg / m2,第1天静脉注射亚叶酸钙200 mg / m2,第1天静脉注射氟尿嘧啶400 mg /通过集中式电子系统连续静脉滴注氟尿嘧啶[2400 mg / m2],每14天重复一次,有或无第5天静脉滴注贝伐单抗5 mg / kg)。
根据以下因素对患者进行分层(日本 vs 韩国 vs 中国);美国东部肿瘤协作组(ECOG)体能状态评分(0 - 1 vs 2);转移部位数量(1处 vs 1处以上);既往接受奥沙利铂治疗(是 vs 否);同时联合贝伐珠单抗治疗(是 vs 否)。
研究结果
2013年12月2日至2015年8月13日期间,650名患者入选并随机分配接受mXELIRI联合或不联合贝伐单抗(n = 326)或FOLFIRI联合或不联合贝伐单抗(n = 324)。在中位随访15.8个月后(IQR 8.7-24.9),总共有490例患者死亡(mXELIRI中有242例患者使用或不使用贝伐单抗组,248例FOLFIRI患者有或无贝伐单抗组)。
mXELIRI组的中位总生存期为16.8个月(95%CI 15.3-19.1),FOLFIRI组为15.4个月(13.0-17.7)(HR0.85, 95%CI 0.71-1.02; pnon-inferiority <0.0001)。
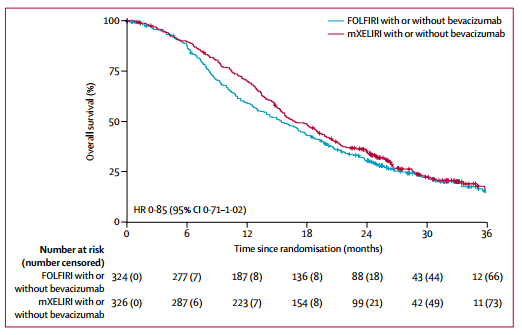
图1 os
同样,两组之间的中位无进展生存无显著差异:mXELIRI组为8.4个月(95% CI = 7.1−9.1),FOLFIRI组为7.2个月(95% CI = 6.6−6.6),HR = 0.95;95% CI = 0.81-1.11;P = 0.5078。
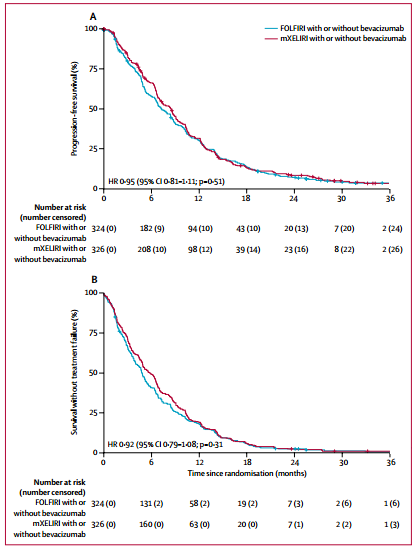
图2 PFS(A)和治疗失败的时间(B)
mXELIRI组的3级/4级不良事件发生率显著低于FOLFIRI组,53.9% vs 72.3%,P<0.0001。最常见的3-4级不良事件是中性粒细胞减少(mXELIRI组310名患者中52名[17%],FOLFIRI组310名133名[43%])。mXELIRI组发生3-4级腹泻的发生率(22 [7%])高于FOLFIRI组(10 [3%])。在mXELIRI组310例患者中有46例(15%)和FOLFIRI组中310例患者中有63例(20%)报告了严重不良事件。在mXELIRI组中观察到两个与治疗有关的死亡(一个肺炎和一个肺部感染),并且在FOLFIRI组中有一个与治疗有关的死亡(肺部感染)。
在所有预先设定的亚组中,疗效和安全性结果相似。
结论
AXEPT研究表明,mXELIRI联合或不联合贝伐珠单抗方案治疗转移性结直肠癌患者的总生存时间不劣于标准FOLFIRI方案。mXELIRI方案可替代标准FOLFIRI方案作为转移性结直肠癌的二线标准治疗方案,至少对亚洲患者群体而言。
参考文献:
Modified XELIRI (capecitabine plus irinotecan) versus FOLFIRI (leucovorin, fluorouracil, and irinotecan), both either with or without bevacizumab, as second-line therapy for metastatic colorectal cancer (AXEPT): a multicentre, open-label, randomised, non-inferiority, phase 3 trial.The Lancet Oncology.16 March 2018.





